29.04.2026 à 09:30
Lessive : Peut-on passer de 50 à 5 ingrédients et toujours avoir un linge propre ?
Texte intégral (1922 mots)

Vous lancez une machine, versez une dose de lessive et attendez un linge propre : taches éliminées, fibres et couleurs préservées, même à basse température. Derrière ce geste quotidien se cache une chimie sophistiquée. Les formulations actuelles mobilisent souvent plus de 30 ingrédients, chacun jouant un rôle précis. Pourtant, on voit apparaître des lessives mettant en avant des listes plus courtes, parfois réduites à moins de 10 composants, portées par une demande de transparence et de moindre impact environnemental. Mais peut-on vraiment simplifier sans perdre en efficacité ?
Une lessive ne se contente pas de nettoyer. Elle doit simultanément décoller les salissures, préserver les tissus et fonctionner dans des eaux de qualité variable. Pour y parvenir, chaque ingrédient remplit un rôle précis. Les tensioactifs forment la colonne vertébrale de la formulation. Leur structure amphiphile – une tête hydrophile avec affinité pour l’eau et une chaîne hydrophobe attirant les graisses – leur permet de s’intercaler entre les salissures et les fibres, de les décoller et de les maintenir en suspension dans le bain de lavage.
Les enzymes complètent cette action en ciblant des taches spécifiques : les protéases décomposent les taches protéiniques (sang, œuf), les amylases s’attaquent aux amidons (sauces, pâtes, riz), tandis que les lipases hydrolysent graisses et huiles. Leur efficacité à basse température explique en grande partie pourquoi les lessives modernes peuvent nettoyer sans chauffer fortement l’eau. D’autres ingrédients assurent des fonctions complémentaires, comme l’efficacité du lavage en eau dure (une eau riche en ions calcium et magnésium, une eau calcaire), la stabilité de la formulation ou la limitation de la redéposition des salissures sur les fibres.
Cette complexité s’est construite au fil des décennies pour répondre à des exigences toujours plus élevées. Certaines fonctions restent difficiles à concilier : améliorer la blancheur peut altérer les couleurs vives, tandis que renforcer l’efficacité à basse température exige souvent des systèmes enzymatiques plus élaborés. Notons que la réglementation européenne n’impose pas l’affichage de la liste complète des ingrédients sur l’emballage, mais seulement des classes de composants avec des fourchettes de pourcentages. Obtenir la liste exhaustive reste souvent complexe pour le consommateur. Si la liste détaillée est théoriquement accessible en ligne, elle est en pratique plus ou moins facile à consulter, parfois dispersée dans des documents techniques.
Les deux moteurs de la simplification
Les formulations tendent aujourd’hui à se raccourcir sous l’effet de deux dynamiques. La première est réglementaire. Ainsi, les phosphates, autrefois largement utilisés comme agents séquestrants, ont été fortement limités puis pratiquement éliminés des lessives ménagères en Europe depuis 2013. Rejetés dans les eaux usées après le lavage, les phosphates contribuent à l’eutrophisation des milieux aquatiques, c’est-à-dire à un enrichissement excessif en nutriments. Ils favorisent ainsi la prolifération d’algues, qui appauvrit l’eau en oxygène et peut entraîner une perte de biodiversité.
La seconde dynamique est sociétale. Une demande croissante de transparence et de réduction de l’empreinte environnementale pousse les fabricants à proposer des formules plus courtes. Azurants optiques, qui donnent une impression de blancheur plus éclatante sans agir directement sur le nettoyage, parfums, conservateurs, remplissent des fonctions réelles, mais sont de plus en plus contestés pour leurs effets allergènes potentiels ou leur persistance dans l’environnement. Certains labels, comme l’Écolabel européen, vont au-delà de la réglementation en les excluant ou en les limitant strictement, privilégiant certains critères écologiques au détriment d’autres performances.
Simplifier, c’est arbitrer
Réduire le nombre d’ingrédients ne consiste pas à supprimer des composants sans conséquence. Il s’agit de recomposer un nouvel équilibre entre contraintes souvent contradictoires.
Le cercle de Sinner, cadre classique en chimie du lavage, illustre ces arbitrages. Il repose sur quatre paramètres interdépendants : action chimique, température de l’eau, temps de contact et action mécanique. Pour obtenir un niveau de propreté donné, ces facteurs se compensent : réduire l’un impose d’en renforcer un autre.
C’est exactement la logique des programmes « éco » des machines à laver : en abaissant la température à 30 ou 40 °C au lieu de 60 °C, ils allongent la durée du cycle. Si cette baisse de température permet de réduire la consommation d’énergie, elle peut rendre aussi le lavage moins efficace, ce qui nécessite des formulations souvent plus sophistiquées, capables d’agir à froid. Le lavage à basse température ne simplifie donc pas nécessairement les formules, et peut au contraire conduire à les complexifier.
Du bidon à la dosette : la complexité change de forme
L’évolution des formats de lessive illustre la manière dont la complexité est parfois redistribuée plutôt qu’éliminée. Les lessives liquides, aujourd’hui dominantes, sont pratiques et efficaces à basse température, mais transportent une part importante d’eau, souvent plus de la moitié de la formulation et nécessitent des conservateurs. Les formats concentrés ou solides visent à réduire l’emballage et l’impact du transport, mais nécessitent un dosage plus précis de la part du consommateur.
Dans ce contexte, le volume du flacon n’est pas toujours un bon indicateur : les fabricants indiquent généralement sur l’emballage le nombre de lavages, qui reflète mieux la concentration et facilite la comparaison entre produits.
Le surdosage reste fréquent : par habitude ou par crainte d’un résultat insuffisant, beaucoup de consommateurs versent plus que la dose recommandée. Au-delà d’un certain seuil, les tensioactifs supplémentaires n’améliorent plus le nettoyage ; ils sont simplement rejetés dans les eaux usées, augmentant inutilement la charge environnementale.
Les dosettes multi-compartiments offrent une autre réponse élégante : en séparant physiquement des ingrédients incompatibles (certaines enzymes et agents oxydants qui se neutraliseraient dans un mélange unique), elles préservent l’efficacité de chacun jusqu’au moment du lavage, tout en imposant une dose prédéfinie qui limite mécaniquement le surdosage. La complexité chimique n’a pas disparu ; elle a simplement été intégrée dans l’architecture du produit.
Performance maximale ou performance suffisante ?
Le véritable enjeu réside ici. Les lessives classiques sont conçues selon une logique de performance maximale : elles doivent venir à bout des situations les plus exigeantes – taches tenaces, eau très calcaire, textiles délicats – même si ces cas restent minoritaires dans la vie quotidienne.
Pourtant, l’Agence de l’environnement et de la maîtrise de l’énergie (Ademe) le rappelle : la très grande majorité du linge porté n’est que peu ou modérément sale, et il est recommandé d’espacer les lavages. Viser systématiquement la performance maximale revient à surdimensionner la formulation pour des usages qui ne le justifient pas. Dans la pratique, pour le linge du quotidien, des doses modérées et des cycles à basse température sont généralement suffisants. À l’inverse, pour des taches plus tenaces – vêtements de sport ou de travail –, il peut être plus pertinent d’avoir recours à des détachants ciblés plutôt que d’augmenter systématiquement les doses de lessive.
Adapter les formulations aux usages majoritaires implique donc de passer d’une approche universelle à une logique de performance suffisante, c’est-à-dire une efficacité adaptée à la grande majorité des lavages quotidiens. Ce n’est pas une régression technique, mais un choix de conception assumé qui rend enfin visibles les arbitrages. Les lessives pour linge blanc (avec agents de blanchiment et azurants optiques) et celles pour linge foncé (sans ces composants pour préserver les couleurs) en sont l’illustration parfaite : on ne peut pas optimiser simultanément ces deux objectifs.
Enfin, le prix joue un rôle important. Les lessives revendiquant une formulation plus simple ou un impact réduit sont souvent plus chères à l’achat que les produits classiques, en raison du coût plus élevé des ingrédients alternatifs d’origine végétale ou biodégradable, des volumes de production généralement plus faibles et des certifications spécifiques. Toutefois, ce surcoût à l’achat ne se traduit pas nécessairement par un coût plus élevé à l’usage. Grâce à une concentration souvent supérieure et à un dosage plus précis, le prix par lavage peut s’approcher, voire s’aligner sur celui des lessives classiques, notamment avec les marques de distributeurs écologiques qui offrent aujourd’hui un excellent rapport qualité-prix.
Au fond, la simplification ne change pas seulement les formules, elle interroge aussi nos habitudes d’usage. Et c’est peut-être là son véritable apport : non pas viser une performance maximale en toutes circonstances, mais ajuster le niveau de performance réellement nécessaire selon les situations.
Véronique Sadtler ne travaille pas, ne conseille pas, ne possède pas de parts, ne reçoit pas de fonds d'une organisation qui pourrait tirer profit de cet article, et n'a déclaré aucune autre affiliation que son organisme de recherche.
28.04.2026 à 15:51
Comment se forment les gouttes de pluie ?
Texte intégral (1411 mots)

Dans leur ouvrage Balade sous la pluie, paru en 2025 aux Presses des Ponts, Auguste Gires, ingénieur en chef du corps des Ponts, eaux et forêts, et chercheur au laboratoire Hydrologie, météorologie et complexité de l’École nationale des ponts et chaussées, et Eleonora Dallan, ingénieure en environnement et chercheuse au département Terre, environnement, agriculture et forêts, de l’Université de Padoue en Italie, nous emmènent en promenade pour découvrir un phénomène très courant, mais finalement peu connu : la pluie.
Pour la quatrième « escale » de ce livre-promenade, ils nous expliquent comment se forment physiquement les gouttes de pluie dans les nuages. Extrait.
N’est-il pas surprenant que tous ces cumulus (nuages cotonneux de basse altitude) semblent se former à la même altitude ? En réalité, cela est lié à la façon dont les nuages, et plus largement les précipitations, sont générés. Sur Terre, les conditions de température et de pression permettent à l’eau d’exister naturellement dans trois états : liquide (comme dans les océans, les rivières, ou l’eau du robinet), solide (tel que la glace, la neige, la grêle, la pluie verglaçante), et gazeuse, dans l’air sous forme de vapeur invisible. Les interactions entre ces trois états sont, entre autres, à l’origine de la pluie.
Les noms des nuages
-
La plupart des noms de nuages comportent des racines et qualificatifs latins,
dont l’association donne une indication sur le type de nuage désigné, notamment :
- STRATUS/STRATO : étendu, couche, continu ;
- CUMULUS/CUMULO : amas, moutonneux ;
- CIRRUS/CIRRO : filament, fin ;
- NIMBUS/NIMBO : porteur de pluie.
- ALTO : moyen (même si altus en latin signifie « haut ») Par exemple, un altocumulus, est un nuage moutonneux de moyenne altitude.
Tout commence par l’évaporation, c’est-à-dire qu’une partie de l’eau liquide présente à la surface de la Terre s’évapore sous l’action du soleil. La vapeur d’eau se mélange à l’air ambiant près de la surface. Cet air, réchauffé par le soleil, devient plus chaud que celui du dessus. Sa masse volumique devient plus faible que celle de l’air qui l’entoure (on dit qu’il est plus léger dans le langage courant), ce qui facilite sa montée. En effet, les molécules qu’il contient bougent plus vite sous l’effet de la chaleur et occupent alors plus de place, tout en gardant la même masse.
En raison de la baisse de la température avec l’altitude, généralement d’environ 6,5 °C tous les 1 000 mètres, l’air initialement chaud se refroidit progressivement en montant. Il s’avère que la quantité de vapeur d’eau que l’air peut contenir diminue avec sa température (environ 7 % par degré). Dans un air plus froid, les molécules sont plus proches les unes des autres, ce qui réduit l’espace disponible pour d’autres molécules de gaz comme la vapeur d’eau. C’est la relation de Clausius-Clapeyron.
Ainsi, à une altitude donnée, qui dépend de la température et de la quantité initiale de vapeur d’eau, l’air devient saturé et ne peut plus contenir autant de vapeur d’eau qu’au moment de l’évaporation, quand l’air était encore proche de la surface. Les spécialistes appellent cela le point de rosée. Une partie de l’eau se condense et retrouve sa forme liquide d’origine. La formation de ces gouttelettes de nuages se fait généralement autour de noyaux de condensation, comme une poussière, de la glace ou du sel. Elles sont beaucoup plus petites que les gouttes de pluie dont nous avons parlé précédemment, avec une taille proche de 0,02 millimètre. Ces gouttelettes sont si petites que les turbulences de l’air ambiant sont suffisamment fortes pour les maintenir en suspension dans l’air, les empêchant de tomber au sol. Cette concentration de gouttelettes dans l’air forme un nuage. Le processus peut également se produire à température négative, et dans ce cas, le nuage est constitué de petits cristaux de glace.
D’une certaine manière, vous êtes tous témoins de la formation de nuages au quotidien. Profitons justement des températures hivernales. Inspirez, expirez… Vous remarquerez qu’une sorte de petit nuage se forme en expirant. Oui, il s’agit bien d’un petit nuage ! L’air qui sort de vos poumons, chaud et humide, rencontre de l’air plus frais dans l’atmosphère extérieure. Une partie de la vapeur d’eau qu’il contient se condense et forme des gouttelettes.
Le même phénomène est à l’œuvre lorsque vous faites bouillir de l’eau. Juste au-dessus de l’eau chaude dans la casserole, l’air est très chaud et contient beaucoup de vapeur d’eau. En remontant, il rencontre de l’air plus frais et une partie de l’eau se condense en gouttelettes. Ce que vous voyez n’est donc certainement pas de la vapeur d’eau, qui est invisible, mais bien un petit nuage.
La quantité d’eau liquide contenue dans les nuages, soit la teneur en eau liquide, varie fortement en fonction du type de nuages. Elle est exprimée en masse d’eau liquide par unité de volume d’air, en gramme par mètre cube (g/m3). Elle présente une très grande variabilité d’un nuage à l’autre, voire au sein d’un même nuage. Les ordres de grandeur peuvent aller de 0,06 g/m3 pour des nuages non précipitants comme les cirrus, des nuages de haute altitude, à 0,4 g/m3 pour des nuages engendrant des pluies, tels que les stratocumulus,** **qui sont à plus basse altitude. Les valeurs sont plus élevées pour les cumulonimbus, dont il sera question lors de la prochaine escale.
Qu’en est-il de la pluie ? Pour qu’elle se forme, il faut que les gouttelettes contenues dans les nuages grossissent de façon à être suffisamment lourdes pour tomber. Cela se produit principalement grâce à deux processus.
Le premier, le processus Wegener-Bergeron-Findeisen, implique la croissance de cristaux de glace dans des nuages en phase mixte. Ces nuages, caractérisés par des températures négatives, contiennent simultanément de l’eau dans ses trois états : de la glace, de l’eau surfondue (de l’eau en dessous de 0 °C, mais pas encore solidifiée) et de la vapeur d’eau. Dans cet environnement sous-saturé en eau liquide, celle-ci s’évapore rapidement, tandis que la vapeur d’eau se dépose tout aussi vite dans les cristaux de glace, entraînant une croissance soudaine de ces derniers. Le deuxième est la coalescence. Dans les nuages contenant assez de gouttelettes, certaines d’entre elles entrent en collision au cours de leur mouvement, fusionnent et grossissent progressivement.
Les auteurs ne travaillent pas, ne conseillent pas, ne possèdent pas de parts, ne reçoivent pas de fonds d'une organisation qui pourrait tirer profit de cet article, et n'ont déclaré aucune autre affiliation que leur organisme de recherche.
27.04.2026 à 15:54
L’oxygène, cette molécule paradoxale, base de la vie et poison mortel : comment les microorganismes y font face
Texte intégral (2293 mots)
Les humains ainsi que bon nombre d’espèces vivantes ont besoin d’oxygène pour vivre. Pourtant cette molécule est chimiquement dangereuse, elle provoque ce que l’on appelle le « stress oxydant » (une altération des constituants de nos cellules comme les protéines ou l’ADN). Il faut donc pouvoir l’utiliser, mais également s’en protéger. Une nouvelle étude éclaire ces processus chez des microalgues.
La relation entre la vie et l’oxygène est loin d’être simple. Pour la comprendre, il faut remonter aux origines de la vie sur Terre, à l’époque archéenne (entre -4 milliards et -2,5 milliards d’années). Les océans existaient déjà, mais l’atmosphère contenait très peu, voire pas du tout, d’oxygène libre.
Certaines bactéries réalisaient déjà une photosynthèse dite anoxygénique qui, contrairement à celle des plantes et des algues actuelles, ne libère pas d’oxygène mais produit des composés soufrés.
Il y a environ 2,4 milliards d’années survient un tournant majeur : la Grande Oxygénation. L’oxygène commence à s’accumuler dans l’atmosphère grâce à l’activité de bactéries photosynthétiques (les cyanobactéries) capables de réaliser la photosynthèse oxygénique, le même processus que celui utilisé aujourd’hui par les plantes et les algues.
Cette accumulation d’oxygène transforme profondément la biosphère. Pour la première fois, une molécule extrêmement réactive est produite en grande quantité par des organismes vivants. L’oxygène peut oxyder et endommager les structures cellulaires des organismes qui n’y sont pas adaptés. La vie se trouve alors confrontée à un paradoxe : devoir composer avec une molécule qu’elle produit elle-même mais qui représente un danger pour la majorité des formes de vie existantes.
Cette transition provoque une crise biologique majeure. De nombreuses espèces anaérobies sont repoussées vers des milieux pauvres en oxygène, comme les sédiments ou les profondeurs marines. Parallèlement, certaines lignées développent des mécanismes capables de neutraliser l’oxygène, puis de l’utiliser comme source d’énergie. La respiration oxygénique, bien plus efficace que les métabolismes anaérobies, permet ainsi l’émergence de formes de vie plus complexes.

Le paradoxe de l’oxygène
Bien que souvent associé à la vie, l’oxygène demeure chimiquement dangereux et peut provoquer ce que l’on appelle le stress oxydant. En effet, le dioxygène peut générer des espèces réactives de l’oxygène (ERO) – superoxyde, peroxyde d’hydrogène ou radical hydroxyle – capables d’endommager protéines, lipides et ADN.
Tous les organismes aérobies (y compris les humains) possèdent donc des systèmes enzymatiques permettant de neutraliser ces molécules : superoxyde dismutases, catalases ou peroxydases. Sans ces mécanismes de défense, l’oxygène serait rapidement létal. La vie moderne repose ainsi sur un équilibre délicat : utiliser l’oxygène pour produire de l’énergie tout en limitant ses effets toxiques.
Longtemps considérées uniquement comme des sous-produits nocifs impliqués dans le vieillissement ou certaines maladies, les ERO sont aujourd’hui reconnues comme des molécules de signalisation participant à la régulation de nombreux processus cellulaires (prolifération cellulaire ou régulation de certains gènes par exemple). Leur rôle exact reste cependant encore largement inexploré.
Le stress oxydant dans les environnements naturels
Le stress oxydant ne concerne pas seulement les organismes humains : il affecte l’ensemble du vivant. Il apparaît lorsque la production d’ERO dépasse les capacités de défense de la cellule. Ce phénomène est particulièrement marqué dans des environnements soumis à de fortes variations de conditions physiques ou chimiques.
Ces milieux extrêmes comme la mer morte, le désert du Sahara ou certains déserts d’altitude recevant un fort rayonnement solaire, possèdent des conditions très salées, très sèches ou fortement irradiées, mais abritent pourtant une biodiversité étonnante. Des organismes spécialisés, appelés extrêmophiles, y prospèrent grâce à des adaptations physiologiques remarquables. La notion d’environnement extrême dépend donc toujours de l’organisme considéré.
Même des milieux plus familiers peuvent imposer des contraintes importantes. Nos zones côtières, par exemple, connaissent des fluctuations rapides de lumière. L’intensité lumineuse y varie fortement au cours de la journée, ce qui influence directement l’activité photosynthétique.
Les organismes photosynthétiques sont particulièrement exposés à ce problème, car la capture d’énergie lumineuse favorise la formation d’espèces réactives de l’oxygène. Ainsi, si la lumière est indispensable à la photosynthèse, un excès d’énergie lumineuse peut perturber l’équilibre cellulaire et favoriser la formation d’ERO. Les organismes doivent donc exploiter la lumière tout en se protégeant de ses effets potentiellement toxiques.
Les adaptations des microalgues aux variations journalières de lumière
Les diatomées, microalgues très abondantes dans les sédiments marins, ont développé plusieurs stratégies pour faire face à ces variations lumineuses. Des pigments protecteurs, notamment les xanthophylles, limitent la formation de radicaux libres. Les cellules peuvent également modifier l’organisation de leur appareil photosynthétique afin d’optimiser la capture de lumière tout en réduisant les dommages.
Ces microalgues possèdent aussi des photorécepteurs capables de détecter les variations lumineuses et de déclencher des réponses physiologiques rapides, comme l’activation de mécanismes de photoprotection ou l’expression de certains gènes.
L’une de leurs adaptations les plus remarquables est leur migration verticale dans le sédiment. Lorsque la lumière est modérée, les diatomées remontent vers la surface afin de maximiser la photosynthèse. Lorsque l’intensité devient trop forte, elles s’enfoncent légèrement dans le sédiment, comme pour se mettre à l’ombre. Ces déplacements sont synchronisés par une horloge circadienne interne qui permet d’anticiper les cycles jour-nuit.
ERO et diatomées : un dialogue plus complexe qu’on ne le croyait
Des travaux récents suggèrent que les espèces réactives de l’oxygène pourraient jouer un rôle plus actif qu’on ne le pensait. Au-delà de leur caractère potentiellement toxique, elles pourraient agir comme signaux déclenchant certaines réponses comportementales.
Notre dernière étude montre que les ERO participent notamment au contrôle de la migration verticale des diatomées, alors que l’on pensait jusqu’à présent que ces migrations servaient principalement à limiter leur production et leur accumulation au niveau cellulaire.
Deux mécanismes semblent donc se combiner : la migration permet de réduire l’exposition à des conditions génératrices d’ERO, mais ces mêmes molécules pourraient également agir comme signaux déclenchant la réponse lorsque leur concentration dépasse un certain seuil.
Ce système fonctionnerait ainsi comme un véritable dispositif de surveillance interne. Les variations du stress oxydant reflètent rapidement les changements de l’environnement et permettent aux cellules d’ajuster leurs réponses physiologiques et comportementales.
Les diatomées étant très diversifiées et largement distribuées à l’échelle globale, il est probable que ces capacités de détection, de traitement de l’information et de mise en place de réponses varient selon les espèces et le contexte environnemental. Cette diversité confère aux diatomées une forte capacité d’adaptation, jouant un rôle essentiel dans leur survie.
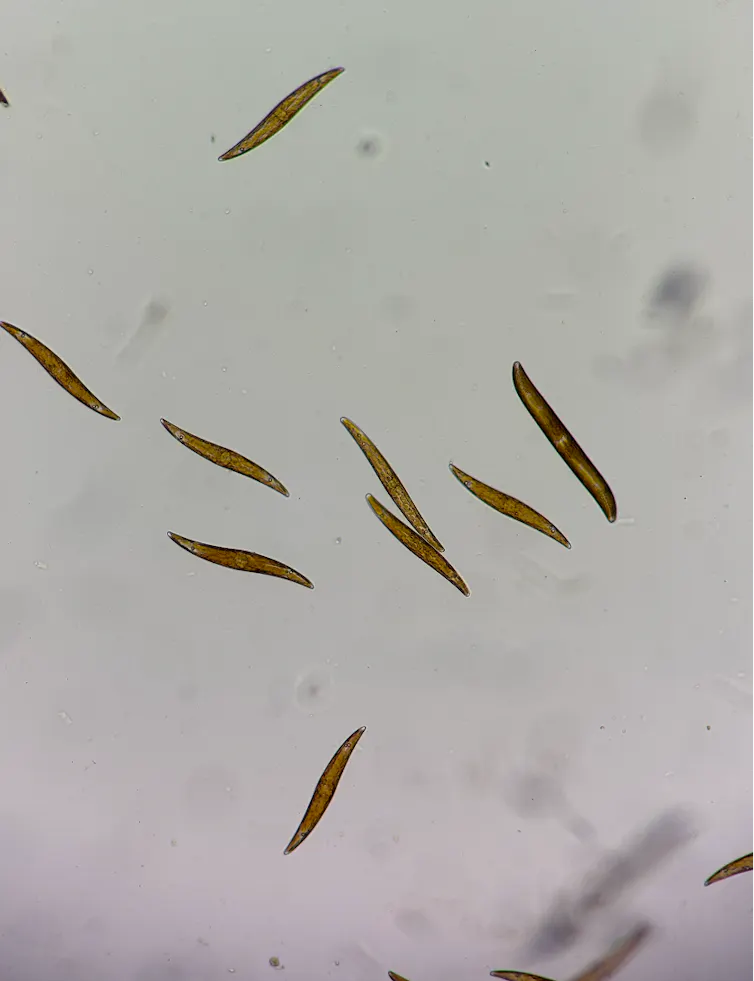
Ce travail montre, à travers un exemple frappant, que le vivant n’a pas seulement appris à se défendre contre l’oxygène et ses dérivés toxiques : il a aussi appris à les utiliser. Des déchets métaboliques oxygénés, autrefois considérés comme uniquement dangereux pour les cellules, peuvent devenir de véritables outils biologiques.
Cela rappelle que le rôle des ERO reste complexe et encore largement méconnu. Loin d’être de simples agents de stress, elles apparaissent aujourd’hui comme des molécules ambivalentes : des messagers subtils intégrés à des mécanismes fins de communication, d’adaptation cellulaire et de perception de l’environnement, notamment chez les diatomées.
Et comme souvent en sciences, ces découvertes ouvrent surtout de nouvelles questions… qui restent encore à explorer.
Nous remercions l’école doctorale DIVONA, la station marine de Concarneau (Finistère) et le laboratoire BOREA.
Alexandre Desparmet a reçu des financements de l'institut de l'Océan de l'Alliance Sorbonne Université.
Cédric Hubas a reçu des financements de l'institut de l'Océan de l'Alliance Sorbonne Université.
