28.04.2026 à 15:51
Comment se forment les gouttes de pluie ?
Texte intégral (1411 mots)

Dans leur ouvrage Balade sous la pluie, paru en 2025 aux Presses des Ponts, Auguste Gires, ingénieur en chef du corps des Ponts, eaux et forêts, et chercheur au laboratoire Hydrologie, météorologie et complexité de l’École nationale des ponts et chaussées, et Eleonora Dallan, ingénieure en environnement et chercheuse au département Terre, environnement, agriculture et forêts, de l’Université de Padoue en Italie, nous emmènent en promenade pour découvrir un phénomène très courant, mais finalement peu connu : la pluie.
Pour la quatrième « escale » de ce livre-promenade, ils nous expliquent comment se forment physiquement les gouttes de pluie dans les nuages. Extrait.
N’est-il pas surprenant que tous ces cumulus (nuages cotonneux de basse altitude) semblent se former à la même altitude ? En réalité, cela est lié à la façon dont les nuages, et plus largement les précipitations, sont générés. Sur Terre, les conditions de température et de pression permettent à l’eau d’exister naturellement dans trois états : liquide (comme dans les océans, les rivières, ou l’eau du robinet), solide (tel que la glace, la neige, la grêle, la pluie verglaçante), et gazeuse, dans l’air sous forme de vapeur invisible. Les interactions entre ces trois états sont, entre autres, à l’origine de la pluie.
Les noms des nuages
-
La plupart des noms de nuages comportent des racines et qualificatifs latins,
dont l’association donne une indication sur le type de nuage désigné, notamment :
- STRATUS/STRATO : étendu, couche, continu ;
- CUMULUS/CUMULO : amas, moutonneux ;
- CIRRUS/CIRRO : filament, fin ;
- NIMBUS/NIMBO : porteur de pluie.
- ALTO : moyen (même si altus en latin signifie « haut ») Par exemple, un altocumulus, est un nuage moutonneux de moyenne altitude.
Tout commence par l’évaporation, c’est-à-dire qu’une partie de l’eau liquide présente à la surface de la Terre s’évapore sous l’action du soleil. La vapeur d’eau se mélange à l’air ambiant près de la surface. Cet air, réchauffé par le soleil, devient plus chaud que celui du dessus. Sa masse volumique devient plus faible que celle de l’air qui l’entoure (on dit qu’il est plus léger dans le langage courant), ce qui facilite sa montée. En effet, les molécules qu’il contient bougent plus vite sous l’effet de la chaleur et occupent alors plus de place, tout en gardant la même masse.
En raison de la baisse de la température avec l’altitude, généralement d’environ 6,5 °C tous les 1 000 mètres, l’air initialement chaud se refroidit progressivement en montant. Il s’avère que la quantité de vapeur d’eau que l’air peut contenir diminue avec sa température (environ 7 % par degré). Dans un air plus froid, les molécules sont plus proches les unes des autres, ce qui réduit l’espace disponible pour d’autres molécules de gaz comme la vapeur d’eau. C’est la relation de Clausius-Clapeyron.
Ainsi, à une altitude donnée, qui dépend de la température et de la quantité initiale de vapeur d’eau, l’air devient saturé et ne peut plus contenir autant de vapeur d’eau qu’au moment de l’évaporation, quand l’air était encore proche de la surface. Les spécialistes appellent cela le point de rosée. Une partie de l’eau se condense et retrouve sa forme liquide d’origine. La formation de ces gouttelettes de nuages se fait généralement autour de noyaux de condensation, comme une poussière, de la glace ou du sel. Elles sont beaucoup plus petites que les gouttes de pluie dont nous avons parlé précédemment, avec une taille proche de 0,02 millimètre. Ces gouttelettes sont si petites que les turbulences de l’air ambiant sont suffisamment fortes pour les maintenir en suspension dans l’air, les empêchant de tomber au sol. Cette concentration de gouttelettes dans l’air forme un nuage. Le processus peut également se produire à température négative, et dans ce cas, le nuage est constitué de petits cristaux de glace.
D’une certaine manière, vous êtes tous témoins de la formation de nuages au quotidien. Profitons justement des températures hivernales. Inspirez, expirez… Vous remarquerez qu’une sorte de petit nuage se forme en expirant. Oui, il s’agit bien d’un petit nuage ! L’air qui sort de vos poumons, chaud et humide, rencontre de l’air plus frais dans l’atmosphère extérieure. Une partie de la vapeur d’eau qu’il contient se condense et forme des gouttelettes.
Le même phénomène est à l’œuvre lorsque vous faites bouillir de l’eau. Juste au-dessus de l’eau chaude dans la casserole, l’air est très chaud et contient beaucoup de vapeur d’eau. En remontant, il rencontre de l’air plus frais et une partie de l’eau se condense en gouttelettes. Ce que vous voyez n’est donc certainement pas de la vapeur d’eau, qui est invisible, mais bien un petit nuage.
La quantité d’eau liquide contenue dans les nuages, soit la teneur en eau liquide, varie fortement en fonction du type de nuages. Elle est exprimée en masse d’eau liquide par unité de volume d’air, en gramme par mètre cube (g/m3). Elle présente une très grande variabilité d’un nuage à l’autre, voire au sein d’un même nuage. Les ordres de grandeur peuvent aller de 0,06 g/m3 pour des nuages non précipitants comme les cirrus, des nuages de haute altitude, à 0,4 g/m3 pour des nuages engendrant des pluies, tels que les stratocumulus,** **qui sont à plus basse altitude. Les valeurs sont plus élevées pour les cumulonimbus, dont il sera question lors de la prochaine escale.
Qu’en est-il de la pluie ? Pour qu’elle se forme, il faut que les gouttelettes contenues dans les nuages grossissent de façon à être suffisamment lourdes pour tomber. Cela se produit principalement grâce à deux processus.
Le premier, le processus Wegener-Bergeron-Findeisen, implique la croissance de cristaux de glace dans des nuages en phase mixte. Ces nuages, caractérisés par des températures négatives, contiennent simultanément de l’eau dans ses trois états : de la glace, de l’eau surfondue (de l’eau en dessous de 0 °C, mais pas encore solidifiée) et de la vapeur d’eau. Dans cet environnement sous-saturé en eau liquide, celle-ci s’évapore rapidement, tandis que la vapeur d’eau se dépose tout aussi vite dans les cristaux de glace, entraînant une croissance soudaine de ces derniers. Le deuxième est la coalescence. Dans les nuages contenant assez de gouttelettes, certaines d’entre elles entrent en collision au cours de leur mouvement, fusionnent et grossissent progressivement.
Les auteurs ne travaillent pas, ne conseillent pas, ne possèdent pas de parts, ne reçoivent pas de fonds d'une organisation qui pourrait tirer profit de cet article, et n'ont déclaré aucune autre affiliation que leur organisme de recherche.
27.04.2026 à 15:54
L’oxygène, cette molécule paradoxale, base de la vie et poison mortel : comment les microorganismes y font face
Texte intégral (2293 mots)
Les humains ainsi que bon nombre d’espèces vivantes ont besoin d’oxygène pour vivre. Pourtant cette molécule est chimiquement dangereuse, elle provoque ce que l’on appelle le « stress oxydant » (une altération des constituants de nos cellules comme les protéines ou l’ADN). Il faut donc pouvoir l’utiliser, mais également s’en protéger. Une nouvelle étude éclaire ces processus chez des microalgues.
La relation entre la vie et l’oxygène est loin d’être simple. Pour la comprendre, il faut remonter aux origines de la vie sur Terre, à l’époque archéenne (entre -4 milliards et -2,5 milliards d’années). Les océans existaient déjà, mais l’atmosphère contenait très peu, voire pas du tout, d’oxygène libre.
Certaines bactéries réalisaient déjà une photosynthèse dite anoxygénique qui, contrairement à celle des plantes et des algues actuelles, ne libère pas d’oxygène mais produit des composés soufrés.
Il y a environ 2,4 milliards d’années survient un tournant majeur : la Grande Oxygénation. L’oxygène commence à s’accumuler dans l’atmosphère grâce à l’activité de bactéries photosynthétiques (les cyanobactéries) capables de réaliser la photosynthèse oxygénique, le même processus que celui utilisé aujourd’hui par les plantes et les algues.
Cette accumulation d’oxygène transforme profondément la biosphère. Pour la première fois, une molécule extrêmement réactive est produite en grande quantité par des organismes vivants. L’oxygène peut oxyder et endommager les structures cellulaires des organismes qui n’y sont pas adaptés. La vie se trouve alors confrontée à un paradoxe : devoir composer avec une molécule qu’elle produit elle-même mais qui représente un danger pour la majorité des formes de vie existantes.
Cette transition provoque une crise biologique majeure. De nombreuses espèces anaérobies sont repoussées vers des milieux pauvres en oxygène, comme les sédiments ou les profondeurs marines. Parallèlement, certaines lignées développent des mécanismes capables de neutraliser l’oxygène, puis de l’utiliser comme source d’énergie. La respiration oxygénique, bien plus efficace que les métabolismes anaérobies, permet ainsi l’émergence de formes de vie plus complexes.

Le paradoxe de l’oxygène
Bien que souvent associé à la vie, l’oxygène demeure chimiquement dangereux et peut provoquer ce que l’on appelle le stress oxydant. En effet, le dioxygène peut générer des espèces réactives de l’oxygène (ERO) – superoxyde, peroxyde d’hydrogène ou radical hydroxyle – capables d’endommager protéines, lipides et ADN.
Tous les organismes aérobies (y compris les humains) possèdent donc des systèmes enzymatiques permettant de neutraliser ces molécules : superoxyde dismutases, catalases ou peroxydases. Sans ces mécanismes de défense, l’oxygène serait rapidement létal. La vie moderne repose ainsi sur un équilibre délicat : utiliser l’oxygène pour produire de l’énergie tout en limitant ses effets toxiques.
Longtemps considérées uniquement comme des sous-produits nocifs impliqués dans le vieillissement ou certaines maladies, les ERO sont aujourd’hui reconnues comme des molécules de signalisation participant à la régulation de nombreux processus cellulaires (prolifération cellulaire ou régulation de certains gènes par exemple). Leur rôle exact reste cependant encore largement inexploré.
Le stress oxydant dans les environnements naturels
Le stress oxydant ne concerne pas seulement les organismes humains : il affecte l’ensemble du vivant. Il apparaît lorsque la production d’ERO dépasse les capacités de défense de la cellule. Ce phénomène est particulièrement marqué dans des environnements soumis à de fortes variations de conditions physiques ou chimiques.
Ces milieux extrêmes comme la mer morte, le désert du Sahara ou certains déserts d’altitude recevant un fort rayonnement solaire, possèdent des conditions très salées, très sèches ou fortement irradiées, mais abritent pourtant une biodiversité étonnante. Des organismes spécialisés, appelés extrêmophiles, y prospèrent grâce à des adaptations physiologiques remarquables. La notion d’environnement extrême dépend donc toujours de l’organisme considéré.
Même des milieux plus familiers peuvent imposer des contraintes importantes. Nos zones côtières, par exemple, connaissent des fluctuations rapides de lumière. L’intensité lumineuse y varie fortement au cours de la journée, ce qui influence directement l’activité photosynthétique.
Les organismes photosynthétiques sont particulièrement exposés à ce problème, car la capture d’énergie lumineuse favorise la formation d’espèces réactives de l’oxygène. Ainsi, si la lumière est indispensable à la photosynthèse, un excès d’énergie lumineuse peut perturber l’équilibre cellulaire et favoriser la formation d’ERO. Les organismes doivent donc exploiter la lumière tout en se protégeant de ses effets potentiellement toxiques.
Les adaptations des microalgues aux variations journalières de lumière
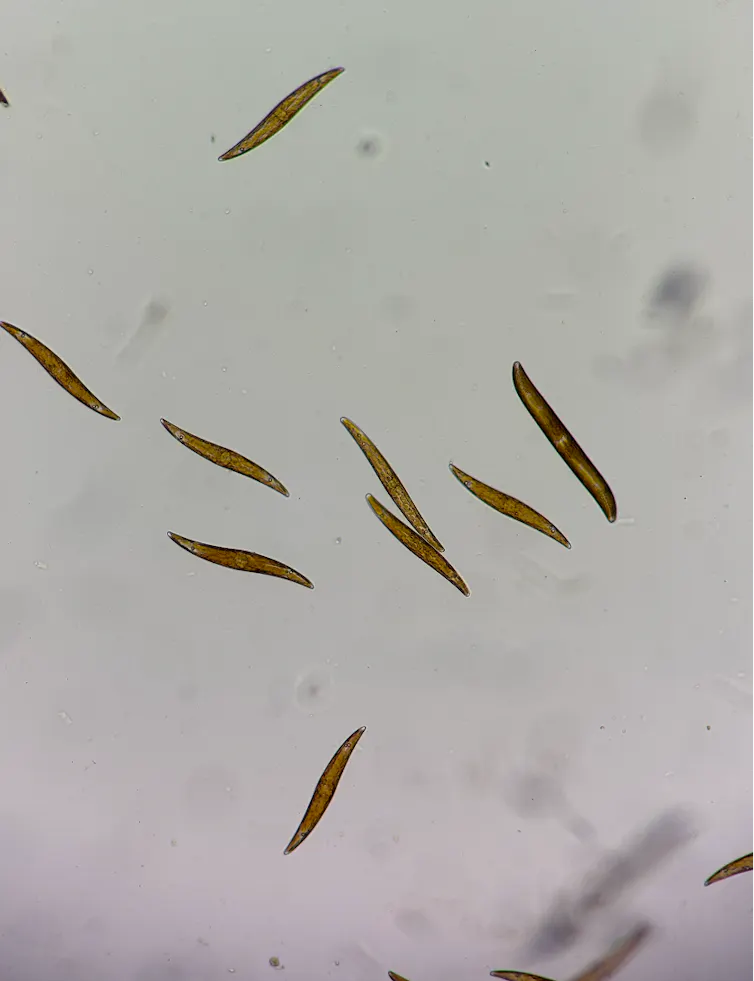
Les diatomées, microalgues très abondantes dans les sédiments marins, ont développé plusieurs stratégies pour faire face à ces variations lumineuses. Des pigments protecteurs, notamment les xanthophylles, limitent la formation de radicaux libres. Les cellules peuvent également modifier l’organisation de leur appareil photosynthétique afin d’optimiser la capture de lumière tout en réduisant les dommages.
Ces microalgues possèdent aussi des photorécepteurs capables de détecter les variations lumineuses et de déclencher des réponses physiologiques rapides, comme l’activation de mécanismes de photoprotection ou l’expression de certains gènes.
L’une de leurs adaptations les plus remarquables est leur migration verticale dans le sédiment. Lorsque la lumière est modérée, les diatomées remontent vers la surface afin de maximiser la photosynthèse. Lorsque l’intensité devient trop forte, elles s’enfoncent légèrement dans le sédiment, comme pour se mettre à l’ombre. Ces déplacements sont synchronisés par une horloge circadienne interne qui permet d’anticiper les cycles jour-nuit.
ERO et diatomées : un dialogue plus complexe qu’on ne le croyait
Des travaux récents suggèrent que les espèces réactives de l’oxygène pourraient jouer un rôle plus actif qu’on ne le pensait. Au-delà de leur caractère potentiellement toxique, elles pourraient agir comme signaux déclenchant certaines réponses comportementales.
Notre dernière étude montre que les ERO participent notamment au contrôle de la migration verticale des diatomées, alors que l’on pensait jusqu’à présent que ces migrations servaient principalement à limiter leur production et leur accumulation au niveau cellulaire.
Deux mécanismes semblent donc se combiner : la migration permet de réduire l’exposition à des conditions génératrices d’ERO, mais ces mêmes molécules pourraient également agir comme signaux déclenchant la réponse lorsque leur concentration dépasse un certain seuil.
Ce système fonctionnerait ainsi comme un véritable dispositif de surveillance interne. Les variations du stress oxydant reflètent rapidement les changements de l’environnement et permettent aux cellules d’ajuster leurs réponses physiologiques et comportementales.
Les diatomées étant très diversifiées et largement distribuées à l’échelle globale, il est probable que ces capacités de détection, de traitement de l’information et de mise en place de réponses varient selon les espèces et le contexte environnemental. Cette diversité confère aux diatomées une forte capacité d’adaptation, jouant un rôle essentiel dans leur survie.
Ce travail montre, à travers un exemple frappant, que le vivant n’a pas seulement appris à se défendre contre l’oxygène et ses dérivés toxiques : il a aussi appris à les utiliser. Des déchets métaboliques oxygénés, autrefois considérés comme uniquement dangereux pour les cellules, peuvent devenir de véritables outils biologiques.
Cela rappelle que le rôle des ERO reste complexe et encore largement méconnu. Loin d’être de simples agents de stress, elles apparaissent aujourd’hui comme des molécules ambivalentes : des messagers subtils intégrés à des mécanismes fins de communication, d’adaptation cellulaire et de perception de l’environnement, notamment chez les diatomées.
Et comme souvent en sciences, ces découvertes ouvrent surtout de nouvelles questions… qui restent encore à explorer.
Nous remercions l’école doctorale DIVONA, la station marine de Concarneau (Finistère) et le laboratoire BOREA.
Alexandre Desparmet a reçu des financements de l'institut de l'Océan de l'Alliance Sorbonne Université.
Cédric Hubas a reçu des financements de l'institut de l'Océan de l'Alliance Sorbonne Université.
26.04.2026 à 09:15
Ce que les créatures des abysses voient dans le noir
Texte intégral (1701 mots)
Dans l’ouvrage Secrets de l’océan profond, tout juste publié aux éditions Quae, Juliette Ravaux, maîtresse de conférences à Sorbonne Université en biologie animale, et Sébastien Duperron, professeur au Muséum national d’histoire naturelle et spécialiste d’écologie microbienne, nous font découvrir des espèces animales mystérieuses et des ressources mal connues de l’océan profond. Leur but est de mieux comprendre ce bien commun, pour mieux le préserver. Dans cet extrait, ces spécialistes nous donnent à voir ce que perçoivent les curieuses espèces vivant dans les abysses, qu’ils ont tous deux pu observer lors de leurs plongées à bord du Nautile, sous-marin de la flotte scientifique à la fois unique… et exigu.
La vie dans l’océan profond s’accompagne d’un panel de contraintes environnementales, parmi lesquelles l’absence de lumière solaire et la rareté de la nourriture. À elles seules, ces deux conditions affectent des fonctions essentielles des organismes telles que l’orientation dans leur environnement à la recherche de nourriture ou de partenaires, mais aussi le métabolisme, la croissance et la reproduction. En conséquence, les espèces des profondeurs possèdent une vaste diversité d’adaptations dont certaines sont présentées ici, mais dont beaucoup restent encore à découvrir !
Descendons sur la dorsale de l’océan Atlantique, à plus de 2 000 mètres de fond, au plus près des fumeurs noirs qui crachent un fluide brûlant. Là, sur les parois des cheminées hydrothermales, des crevettes se rassemblent par milliers en nuées grouillantes. Ce sont des crevettes aveugles, Rimicaris exoculata, une espèce emblématique de ces environnements atlantiques. Les adultes ne possèdent pas les yeux pédonculés typiques des crevettes, ce qui leur vaut ce surnom. Et pourtant, elles possèdent bien des yeux, difficilement reconnaissables car ils sont très modifiés : ce sont des plaques rosées en forme de V qui se situent sur leur dos. Ces plaques ne leur permettent pas de voir leur environnement sous forme d’une image comme le font nos yeux.
Mais elles sont très sensibles à la lumière et détectent des sources lumineuses de très faible intensité, invisibles pour l’œil humain. Elles sont constituées d’une couche très épaisse de cellules photoréceptrices, sous laquelle se trouve une couche réfléchissante de cellules blanches qui renvoie la lumière vers les photorécepteurs, augmentant ainsi la quantité de lumière perçue.
Grâce à ces capteurs hypersensibles, les crevettes Rimicaris sont donc spécialisées dans la détection de lumière ténue. Reste encore à déterminer quels signaux lumineux elles perçoivent dans leur environnement parmi les sources potentielles, comme celle émise par le fluide hydrothermal sous forme de rayonnement thermique.
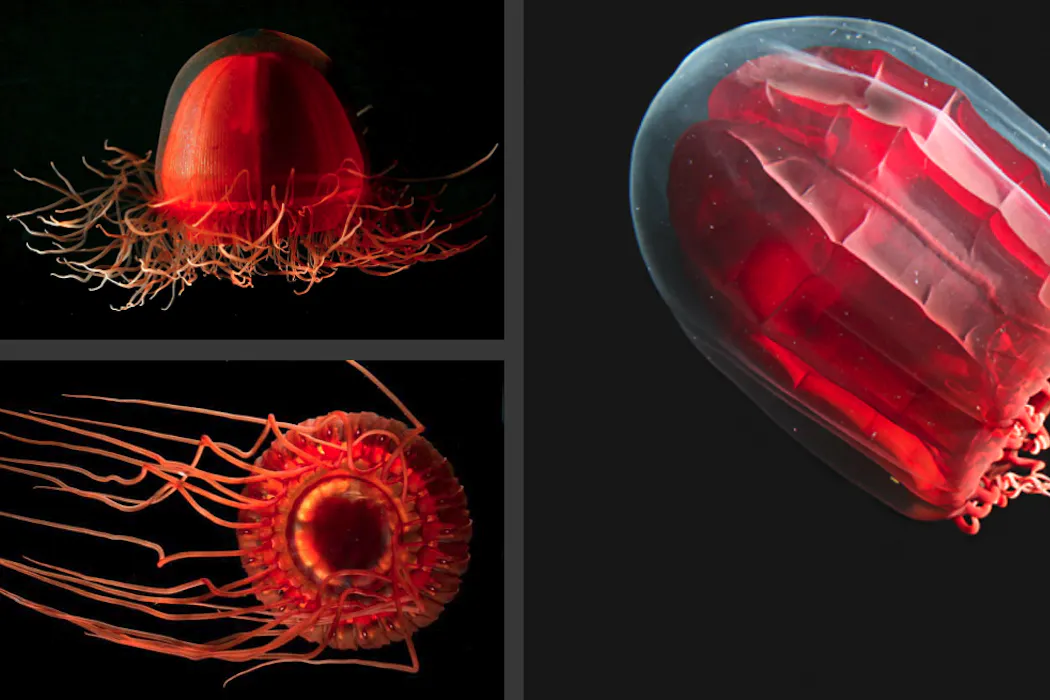
Les animaux bioluminescents, ou pourquoi il ne fait pas totalement noir dans les abysses
À l’instar de Rimicaris, les espèces abyssales évoluent dans des environnements obscurs dépourvus de lumière solaire. Il existe cependant une autre source lumineuse majeure : la bioluminescence. Plus faible que la lumière solaire, elle n’est apparente que la nuit dans les eaux de surface, mais elle est nettement visible en profondeur grâce au contraste avec le fond noir. Cette lumière émise par les organismes révèle la présence de partenaires, de prédateurs, de sources de nourriture, et peut aussi servir de défense, de leurre ou de camouflage. Dans la zone crépusculaire, diverses espèces arborent ainsi un ventre bioluminescent qui les rend moins visibles aux prédateurs et aux proies situés en dessous. Cette contre-illumination leur permet en effet de se fondre dans la faible luminosité provenant de la surface.
Au-delà de 1 000 mètres, la bioluminescence constitue la principale, sinon la seule, source de lumière. Elle apparaît de façon intermittente sous forme d’éclairs lumineux, le plus souvent de couleur bleue ou verte, qui durent quelques dixièmes de secondes à quelques secondes. Des observations menées au large de New York dans les années 1950 rapportent des fréquences de signaux bioluminescents allant jusqu’à 94 éclairs par minute dans le champ de vision du photomètre pour des profondeurs au-delà de 1 000 mètres. Dans les années 2000, un inventaire de la faune au large de la côte californienne, de la surface jusqu’à 3 900 mètres de profondeur, a révélé que plus de trois quarts des individus de la colonne d’eau émettent de la lumière. Les océans crépitent d’un feu d’artifice silencieux et le paysage lumineux des profondeurs se présente comme un fond noir piqueté d’étincelles bleutées.
Les yeux adaptés aux paysages obscurs
Dans ces paysages obscurs, les animaux sont-ils aveugles ? Les yeux des poissons téléostéens peuplant les profondeurs sont souvent décrits comme étant « régressés » ou « dégénérés ». Pourtant, ces yeux existent bel et bien et les poissons des profondeurs ne sont généralement pas aveugles, bien au contraire. Les yeux des poissons bathypélagiques présentent une grande variété de morphologies : ils sont parfois clairement régressé avec une rétine absente ou défectueuse, comme chez les « poissons-baleines » du genre Cetomimus, ou au contraire très grands et développés, comme ceux de l’alépocéphale à bec (Alepocephalus rostratus).
Dans l’ensemble, à quelques exceptions près, les yeux des espèces bathypélagiques ont toutefois tendance à être plus petits (par rapport à la taille du corps) que ceux de leurs cousins de la zone mésopélagique. Ils sont néanmoins parfaitement fonctionnels et particulièrement efficaces pour détecter des éclairs de bioluminescence ponctuels, grâce à deux caractéristiques notables : une large pupille et une rétine riche en photorécepteurs très sensibles à la lumière. Le record est actuellement détenu par la dirette argentée, une espèce abyssale qui possède un nombre exceptionnel de pigments responsables de la détection de faible luminosité, les rhodopsines. Alors que l’humain ne possède qu’un seul exemplaire de rhodopsine, la dirette en possède 38 ! Chacune de ces rhodopsines serait capable de détecter une couleur dans la gamme des bleus et des verts. Cet exceptionnel répertoire de pigments permet donc à la dirette de distinguer davantage de nuances de lumière bleue et de lumière verte que l’être humain, ce qui s’avère très utile pour identifier différentes sources de bioluminescence, et ainsi distinguer les prédateurs et les proies.
Comme la dirette, la majorité des poissons des grands fonds possède une vision limitée aux longueurs d’onde bleues et vertes. Ils ne peuvent percevoir les autres couleurs, et sont de ce fait daltoniens ! Les poissons bathypélagiques seraient en théorie capables de voir un flash bioluminescent à une distance pouvant aller jusqu’à 100 mètres dans une eau limpide. Cependant, cette distance est en réalité inatteignable pour la plupart des poissons pélagiques, qui n’ont pas l’énergie suffisante pour nager jusqu’à une source lumineuse à une telle distance en un laps de temps court. Ainsi, même si les poissons des profondeurs peuvent voir des éclairs lointains, ils ne réagissent probablement qu’à ceux produits à une distance plus proche.
Tout comme les poissons bathypélagiques, les crustacés de ces profondeurs présentent une grande variété de morphologie des yeux. Là encore, on retrouve des exemples d’yeux particulièrement sensibles à la lumière et adaptés à la détection de la bioluminescence. Le record revient probablement aux grands yeux de l’ostracode Gigantocypris muelleri, qui possèdent des réflecteurs qui ressemblent à des phares de voiture et des photorécepteurs géants qui lui confèrent une sensibilité à la lumière impressionnante. Il est ainsi capable de distinguer les silhouettes de proies et de prédateurs qui se profilent contre la faible lumière descendant dans la colonne d’eau au-dessus de lui, et il peut déjouer le camouflage en contre-illumination des espèces bioluminescentes de la zone crépusculaire. S’il est capable de détecter efficacement la bioluminescence, ce crustacé ne peut en revanche voir avec précision l’organisme qui la produit, car ses yeux possèdent une faible résolution, ce qui fait qu’il voit flou !
Dans les grands fonds, on trouve donc des espèces dont la vision s’est adaptée pour percevoir de très faibles intensités lumineuses, et dans un répertoire de couleurs spécialisé, plutôt que pour produire une image nette et détaillée de leur environnement.
Les auteurs ne travaillent pas, ne conseillent pas, ne possèdent pas de parts, ne reçoivent pas de fonds d'une organisation qui pourrait tirer profit de cet article, et n'ont déclaré aucune autre affiliation que leur organisme de recherche.
